发布时间:2019-03-18 17:01:00 浏览 次
作者:郝凤阳,苏健,孙璐,高冠岳
单位:北京市医疗器械检验所材料二室
〔关键词〕人工心脏瓣膜;机械瓣;生物瓣;介入瓣;组织工程瓣
〔中图分类号〕R318.08 〔文献标识码〕A
〔文章编号〕1002-2376(2017)13-0186-06
心脏瓣膜是保证心脏推动血液循环定向流动的生物阀门。心脏瓣膜的病变影响人体正常血液循环,严重者甚至危及生命。人工心脏瓣膜是指用机械或者生物组织材料加工而成的一种用来治疗心脏瓣膜疾病或缺损的心脏植介入医疗器械,是治疗先天性畸形及风湿性心脏病、心脏退化以及细菌感染等疾病所造成的后天性心脏瓣膜疾病引发的心脏瓣膜功能异常的重要治疗手段[1]。
1 人工心脏瓣膜的历史回顾
为治疗心脏瓣膜病变,医学与科学界经历了漫长的探索时期。许多学者都曾试用“瓣膜部分替换术”,但是均以失败告终。之后又尝试进行“非原位瓣膜替换术”的探索[2]。
人工心脏瓣膜的研制历史可以追溯到 20 世纪 40 年代,Hufnagel 等最早开始进行相关的研究工作,
1950 年,Hufnagel 和 Campbell 尝试为患者在离开心脏约 10 cm 的主动脉血管内安放一个人工阀门结构,但是手术没有成功。
1951 年,Hufnagel 为治疗主动脉瓣封闭不全将人造主动脉瓣膜植入患者的主动脉内,但是效果并不理想[3]。
1952 年,Hufnagel 采用甲基丙烯酸球制造出新的阀门结构,并放置于患者降主动脉中用来治疗主动脉关闭不全,患者存活了几个小时。
1960 年,Harken 等首先用人造球笼瓣植入人体主动脉瓣生理位置并获得成功[4],同年,Starr 用改进的球笼瓣成功为患者实施了二尖瓣置换术[5],从此开创了利用人工心脏瓣膜治疗心脏瓣膜疾病的新时代。
1964 年出现了笼碟瓣,其成为第二代人造机械瓣膜。
1969 年,Bjork-Shiley 斜碟瓣问世以来,叶片构型多次进行改进,最大开口可增大到 60°左右,明显降低了阻力,提高了瓣膜性能,这也是当时在临床中应用最为普遍的机械瓣膜之一。
20 世纪 80 年代机械瓣有了突破性进展,即将单叶斜片式机械瓣改为双叶式,这样使得叶片对血流的影响更小,近似于正常心脏瓣膜的中心流型[6],其代表人工心脏瓣膜有 St.Jude 机械瓣、Carbonmedics 机械瓣等。生物瓣的发展几乎与机械瓣同步,起初生物瓣采用福尔马林处理的方法,对瓣叶纤维组织破坏较大,以至于瓣膜很快发生钙化现象。
1968 年,Carpentier 使用戊二醛处理生物瓣,这使得生物瓣的使用寿命大大延长,于是以戊二醛高压固定为标志的第一代生物瓣膜开始广泛应用于临床。第二代生物瓣为更好的保留瓣叶组织以及纤维的排列结构从而延长瓣膜的使用寿命而采用低压或无压固定方式。第三代生物瓣膜加入了抗钙化的处理,这有望使得生物瓣的使用寿命延长到 20 年。
21世纪,介入心脏病学迅速发展,2002年,Cribier 等报道了世界上第一例经导管植入主动脉瓣的人体试验结果[7],这引起了广泛的关注。经导管介入瓣膜治疗方法的出现开创了经导管瓣膜置换的新时代。
美国波士顿市生物科学家们开发出了组织工程人工心脏瓣膜(tissue engineered heart valve,TEHV)[8-9],即利用患者自身细胞经人工培育后成为新的用于置换损坏心脏瓣膜的人工心脏瓣膜。这将是未来最有希望得到大规模利用的心脏瓣膜。
我国也早从 20 世纪 60 年代起便开始了人工心脏瓣膜的相关研究,1965 年蔡用之教授成功运用国产球笼瓣进行二尖瓣置换术[10]。
1975 年广东心血管病研究所引进了国外技术 , 采用进口人工机械瓣进行人工心脏瓣膜置换术。
1976年北京阜外医院成功研制出生物材料人工心脏瓣膜并成功进行主动脉瓣膜替换手术。
1978年上海医疗器械研究所、兰州碳素厂与上海长海医院合作研制的各向同性碳斜碟瓣(B-S 瓣)应用于临床。
1985年航天部703所与中国医学科学院阜外医院合作,开发出 GK(钩孔)型机械瓣膜[11]。
1987年兰州新兰仪表厂等研制出 C-L 型标准瓣,其后又推出改进型 C-L 短柱瓣[12]。
1992 年田子朴等报告国产双叶瓣的临床初步应用结果[13]。
2005 年北京思达医用装置有限公司和空军总医院共同研制的 GK 双叶瓣获得国家药监局准产注册,开始了临床应用。
2 人工心脏瓣膜应满足的条件
人工心脏瓣膜是指用机械或者生物组织材料加工而成的一种用来治疗心脏瓣膜疾病或缺损的心脏植介入医疗器械,标准的人工心脏瓣膜不包括部分瓣叶的置换、带瓣的外通道或装有人造心瓣的人工心脏。人工心脏瓣膜应满足3 个条件:
(1 )可替代病损心脏瓣膜的功能;
(2 )取代病损心脏瓣膜的结构;
(3 )能移植于心脏瓣膜的生理位置上。
一个理想的人工心脏瓣膜应满足如下条件。
(1 )符合心脏瓣膜生物流体力学的要求。即瓣膜开放阻力最小,瓣膜开放时间短,瓣口两侧无明显压力差。当瓣膜关闭时,瓣口关闭速度快、关闭严、无反流。血液通过瓣口产生的流场近似于生理血液流场,不产生涡流。
(2 )材料以及结构机械性能稳定,具有较好的耐久性,在数十年的使用时
间内保持瓣膜的相应功能。
(3 )与肌体组织和血液的相容性好。不破坏血液成分、不凝血、不溶血、不引起机体免疫反应,以及没有噪声,不影响患者的正常生活。
(4 )瓣膜的设计与制造便于外科移植手术的实施,其灭菌、保存方便,手术操作简便易行。
(5 )材料易得,便于制造,价格合理,容易推广。
3 人工心脏瓣膜的种类
人工心脏瓣膜主要分为以下4类:机械瓣膜、生物瓣膜、介入瓣膜、组织工程瓣膜。下面分别就每种瓣膜的特点进行阐述。
3.1 机械瓣膜
3.1.1 机械瓣膜的材料
机械瓣膜是由人工材料制成的心脏瓣膜,其可植入心脏内代替心脏瓣膜,使得血液单向流动,并具有天然心脏瓣膜的功能。机械瓣膜的材料一般包含 3 个部分,即用于制作支架的坚硬材料、用于制作阻塞体的弹性材料以及用于制作瓣环的织品类材料。
机械瓣上所用的坚硬材料应为高度光滑的材料,并且不起反应,应将暴露的表面积和血栓形成率降低到最低。常用的坚硬材料包括金属材料和非金属材料。金属材料主要有:钴铬镍合金,其可以植入人体长期不变并且能够高度抛光;钛,其优于钴铬镍合金,不必铸造,可以采用机械加工的形式,非常惰性并且能够高度抛光。非金属材料主要有 Delrin,它是一种聚缩醛树脂,其缺点是轻度吸水;Teflon,虽然软而且缺乏结构强度,但是证明也可以使用;超高低密度聚乙烯和聚丙烯,可以加压消毒并且极其稳定,但是需要采取浇铸技术进行制造;另外,聚四氟乙烯也是一种很好的材料[14]。
美国 Dowcorning 公司特别制造的硅橡胶是最令人满意的弹性体,1961 年,Storr-Edwords 用其制造成了球形瓣膜。广泛用于心脏瓣膜的材料是由 Guif 原子总公司所发明的各相同性热解碳,其具有玻璃样的外形,并且具有化学惰性,强度高,在模拟机械疲劳试验中可以耐受 973 000 000 次冲击,相当于人体 30 年的心跳次数,能够符合心脏瓣膜的牢固度要求,它既可以作为活动部件,又可以作为支架,缺点是这种材料不能进行机械加工,而需要特别的加工技术。
织品采用涤纶长丝编织而成,用涤纶线牢固地扎在瓣架的凹槽内,具有不皱、不缩、不变形、尺寸稳定等特点,被周围的组织包埋后,更能使其牢固地固定。
3.1.2 机械瓣膜的类型
机械瓣膜主要有 4 种类型:球笼瓣、笼碟瓣、斜碟瓣、双叶瓣。其发展历程见表 1。典型的机械瓣膜见图 1。4 种类型的机械瓣膜各有其特点,表 2 就其特点和优缺点分别进行阐述。


3.1.3 机械瓣局限性及发展
机械瓣材料存在血液相容性问题,所以植入机械瓣的患者,必须终身服药进行抗凝治疗。为了降低机械瓣形成血栓的问题,有学者采用离子束沉积方法改善热解碳的血液相容性问题。
随着人工生物材料的发展,有些研究单位研制了人工柔性瓣叶心脏瓣膜(synthetic flexible leaflet heart valve)。这种瓣膜采用血液相容性良好的柔性高分子材料聚氨酯,植入后只需少量或不需进行抗凝治疗。它采用了三个聚氨酯瓣叶结构,瓣口流道具有中心流结构,具有良好的血流动力学特性。瓣叶由三个对称钛合金支架支持,是用高分子聚氨酯一次模压成型的整体结构产品。
3.2 生物瓣膜
现市场占有率较大的另一类人工心脏瓣膜为生物组织瓣,不同于机械瓣全部采用人造材料,生物组织瓣部分或全部采用生物组织材料。生物瓣通常具有良好的生物相容性,不需要长期进行抗凝治疗;置换后血流动力学特性接近人体正常情况;能长期维持组织与功能的完整性。
3.2.1 生物瓣膜的材料
生物组织瓣主要分为同种生物瓣和异种生物瓣两种。
材料来源分为:
(1 )同种同体组织:肺动脉、阔筋膜等;
(2 )同种异体组织:动脉瓣、阔筋膜、硬脑膜等;
(3 )异种异体组织:猪主动脉瓣、牛主动脉瓣、猪心包、牛心包等,其中以猪主动脉瓣最为常见,其次是牛心包瓣[15]。典型的生物瓣膜见图 2。
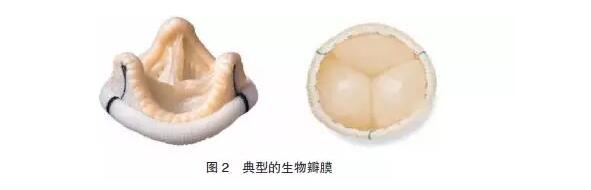
3.2.2 生物瓣膜的发展
生物瓣膜目前已经发展到第三代,见表 3。

3.2.3 生物瓣膜的优缺点
生物瓣的优点:
(1 )抗凝血性好,不易形成血栓和栓塞,术后抗凝治疗 6 个月即可,不必再服用抗凝血药物;
(2 )置换后血流动力学特征接近人体正常情况,血栓形成的可能性非常低,并且不会对血液成分产生破坏;
(3)瓣膜材料血液相容性良好,不会产生凝血、溶血现象,形成血栓的风险较低,能长期维持组织与功能的完整性。生物瓣的缺点是强度较差,瓣膜耐久性比机械瓣短,预期使用寿命一般是 15~20 年。目前,生物瓣膜面临的最大问题是钙化问题,钙化导致材质弹性、韧性以及机械强度都发生很大变化从而造成生物瓣失灵。
3.3 介入瓣膜
经导管植入式人工心脏瓣膜介入治方法的出现,开创了经导管瓣膜置换的新时代。相对于外科手术,支架瓣膜介入治疗方法创伤小、不留疤痕、术后恢复快,因而造福很多患者。典型的介入瓣膜见图3。对比典型的介入支架瓣膜特点,见表4。

3.4 组织工程瓣膜
组织工程瓣膜能创造出一种活的心脏瓣膜.有着良好的自我修复、重建能力,可以克服目前人工心脏瓣膜的各种缺点。它是用人工合成可吸收的聚合物支架或去细胞生物支架,先种植纤维细胞,再种植单层内皮细胞对其进行包裹覆盖[16-18]。
3.4.1 组织工程瓣膜的材料
组织工程支架所用材料及特点见表 5。种子细胞的选择在组织工程瓣膜中尤为重要,目前研究的可以应用于组织工程瓣膜的细胞见表 6。

3.4.2 需重点关注的问题
支架问题:天然材料是良好的支架材料,具有生物相容性好、无免疫原性、无毒性并且适合于细胞黏附、增殖等特点,具有如某些氨基酸序列等细胞识别信号,利于细胞黏附、增殖、分化,但是天然材料受其来源、保存以及伦理等条件的限制,不利于进行机械强度和降解速度的人为调控,不利于在大规模生产,人工合成的聚合物避免了上述限制,但缺乏细胞识别信号,同时与细胞间缺乏良好的生物性相互作用,在应用过程中出现亲水性差,细胞黏附力较弱;机械强度不足;引起无菌性炎症反应等不利因素[19-20]。
种植细胞与基质材料的黏附力问题:细胞与支架材料间的黏附与否是组织工程瓣膜是否成功的基础,这也是实际研究中必须考虑到的问题。实验与临床问题:材料的本构方程只能通过实验来证实。生物瓣膜作为一种软组织材料其力学特征表现为黏弹性及大变形,它的应力 - 应变本构方程应通过实验来确定。
4 人工心脏瓣膜检测标准
随着人工心脏瓣膜技术的不断进步,各种类型的瓣膜不断发展,同时,新型瓣膜也不断问世,国际和国内监管力度也不断增强,相应的检测标准陆续出台,为保证人工心脏瓣膜产品的安全、有效提供依据。目前相关的标准情况见表 7。
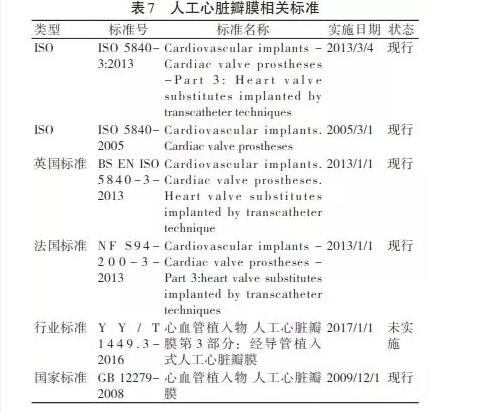
5 结论与讨论
心脏瓣膜疾病是一类危及人类健康和生命的疾病,严重影响患者的工作和生命质量。随着我国经济的快速发展,人民生活水平的提高,医疗保障体系的逐步完善,我国心脏瓣膜替换患者的数量也逐渐增加。人工心脏瓣膜经历了机械瓣、生物外科瓣、介入瓣、组织工程瓣的发展历程,无论采用哪种人工心脏瓣膜,都需要做到安全、有效。目前国内外企业和科研单位大力研究新型介入瓣膜和组织工程瓣膜。随着可降解支架技术的发展,将会更加促进介入瓣膜的发展。从注册检测及技术审评角度,也应紧跟技术发展的步伐,在保证产品安全、有效的前提下,促进人工心脏瓣膜领域从想法、技术到产品的转变,从而为更多的患者带去更为切实有效的治疗方法。
[参考文献]
[1]杨子彬 . 人工心脏瓣膜研究的进展 [J]. 现代临床医学生物工程学杂志,1995,1(1):7-9.
[2]徐向明 . 人工心脏瓣膜及其进展 [J]. 济宁医学院学报,1991,14(2):60-64.
[3]Hufnagel CA. Aortic plastic valvular prosthesis[J]. Bull Georgetown Univ Med Center, 1951,4(5): 128-130.
[4]Harken DE, Soroff HS, Taylor WJ, et al. Partial and complete prostheses in aortic insufficiency[J]. J Thorac Cardiovasc Surg, 1960(40): 744-762.
[5]Starr A, Edwards ML. Mitral replacement: clinical experience with a ball-valve prosthesis[J].Ann Surg, 1961, 154(4): 726-740.
[6]Cimbollek M, Nies B, Wenz R, et al. Antibiotic-impregnated heart valve sewing rings for treatment and prophylaxis of bacterial endocarditis[J]. Antimicrob Agents Ch, 1996, 40(6): 1432-1437.
[7]Cribier A, Eltchaninoff H, Bash A, et al. Percutaneous transcatheter implantation of an aortic valve prosthesis for calcific aortic stenosis: first human case description[J]. Circulation, 2002, 106(24):3006-3008.
[8]Houstrop SP, Kadner A, Melnitchouk S, et al. Tissue engineering of functional trileaflet heart valves from human marrow stromal cells[J]. Circulation, 2002, 106(Suppl I): 143-150.
[9]Hoerstrup SP, Sodian R, Daebritz S, et al. Functional living trileaflet heart valve grown in vitro[J]. Circulation, 2000, 102(Suppl III) :44-49.
[10]张宝仁,朱家麟 . 人造心脏瓣膜与瓣膜置换术 [M]. 北京:人民卫生出版社,1999.
[11]仲京,刘旸,解士胜,等 . 人工机械心脏瓣膜的发展与展望 [J].透析与人工器官,2006,17(1):22-26.
[12]樊庆福 . 人工心脏瓣膜 [J]. 上海生物医学工程,2004,25(4):47-51.
[13]田子朴,罗传兴,黄旭中,等 . 双叶机械瓣的研制和临床应用初步报告 [J]. 中华胸心血管外科杂志,1992,8(1):1.
[14]崔永春,刘晓鹏,张宏,等 . 不同种类人工心脏瓣膜的比较及其生物学评价 [J]. 中国医疗器械信息,2016,(01):2-7,14.
[15]吕昔琴 . 天然交联剂交联制备人工生物心脏瓣膜的研究 [D]. 上海:华东师范大学,2009.
[16]Diemert P, Lange P, Greif M, et al. Edwards Sapien XT valve placement as treatment option for aortic regurgitation after transfemoral CoreValve implantation: a multicenter experience[J]. Clin Res Cardiol, 2014, 103(3):183-190.
[17] Binder RK, Rodés-Cabau J, Wood DA, et al. Edwards SAPIEN 3 valve[J]. Eurointervention, 2012,8(Q): Q83-Q87.
[18]Falk V, Walther T, Schwammenthal E, et al. Transapical aortic valve implantation with a self-expanding anatomically oriented valve[J]. Eur Heart J, 2011,32(7):878-887.
[19]Bijuklic K, Tuebler T, Reichenspurner H, et al. Midterm stability and hemodynamic performance of a transfemorally implantable nonmetallic, retrievable, and repositionable aortic valve in patients with severe aortic stenosis. up to 2-year follow-up of the direct-flow medical valve: a pilot study[J]. Circ Cardiovasc Interv, 2011, 4(6):595-601.
[20]Treede H. Safety and efficacy outcomes from the multicenter CE

欢迎关注《医疗装备》官方公众号