发布时间:2017-08-24 10:02:09 浏览 次
作者:曹宝平 1 ,马超 2 ,匡秋江 3 ,罗刚 4
单位:赣州市人民医院 1 体检科,2 药剂科,3 老年科,4 心内科 (江西赣州 341000)
〔关键词〕注射液;氨基酸;稳定性
〔中图分类号〕R286.0 〔文献标识码〕B
〔文章编号〕1002-2376(2017)15-0001-02
基金项目:赣州市科技局2016年指导性科技计划项目(GZ2016ZSF154)
参附注射液主要用于阳气暴脱的厥脱症,也可用于阳虚所致的惊悸、痹证等;复方氨基酸(18AA- Ⅶ)注射液用于创伤、感染、外科手术后消化系统功能障碍的营养支持; 两种药物联合用于大型创伤患者手术前后营养支持治疗 [1-5], 但是两种药物能否配伍使用,目前尚未有相关资料可供参考。为给临床应用提供依据,本研究对两种药物配伍稳定性进行了分析,现报道如下。
1 仪器与材料
1.1 仪器与试药
高效液相色谱仪(美国 Waters,型号:510 );色谱工作站(江西创新信息工程有限公司,型号:N2000 );超声清洗器(南通市精工仪器有限公司,型号:KQ-100E); pHS-3C 酸度计(上海雷磁仪器厂);人参皂苷 Rg1(中检 所,批号:0710-200621 )和人参皂苷 Re(中检所,批号: 110756-200618 );甲醇、乙腈、磷酸为色谱纯。
1.2 试样样品
复方氨基酸(18AA- Ⅶ)注射液(500 ml,三菱制药, pH 5.1,批号 51570 );参附注射液(雅安三九药业有限公 司,规格 10 ml,批号 31217,pH 5.6 )。
1.3 方法
根据参附注射液说明书临床使用剂量为,一次20~100 ml (用5%~10% 葡萄糖注射液 250~500 ml稀释后使用 ), 静脉滴注。制成单次最大浓度及单次最小浓度的参附注射液,在相同实验条件下同时进行其与复方氨基酸(18AA- Ⅶ)注射液配伍稳定性研究。
单次最大浓度溶液制备:取参附注射液 1000 ml 加入复方氨基酸(18AA- Ⅶ)注射液中,搅匀制成备用。
单次最小浓度溶液制备:取参附注射液 200 ml 加入 5000 ml 复方氨基酸(18AA- Ⅶ)注射液中,搅匀制成备用。
1.4 外观及 pH
在室温 23 ℃条件下,参照中国药典[6-8]将 1.3 下溶液储 存,于配伍后在 0,1,2,4,6 h 进行目视观察性状及检查 可见异物,同时测定各组溶液的 pH,每个样本连测 3 次, 取平均值。
1.5 含量测定
参照参附注射液质量检测标准[8]进行含量测定。
2 结果
2.1 外观性状及可见异物
各配伍溶液外观性状及可见异物检测结果均符合药典规定,见表 1。
表 1 各配伍溶液外观性状及可见异物
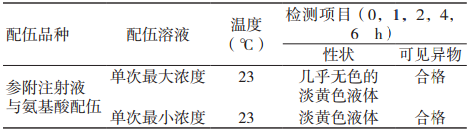
2.2 pH 比较
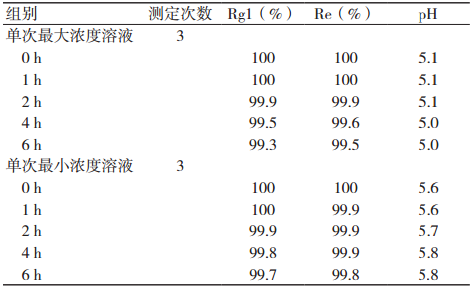
各配伍溶液在 0,1,2,4,6 h,pH 未有显著变化,见表 2。
表 2 Rg1和Re含量及pH[(20±1)℃]
2.3 含量比较
2.3.1 系统适应性
分别取对照品溶液、供试品溶液、空白样品溶液各20 μl 进 样,以人参皂苷 Rg1 和人参皂苷 Re 的峰记,理论塔板数为 1897,分离度为 1.9。
2.3.2 线性关系考察
以浓度(X)为横坐标,以峰面积(Y)为纵坐标,回 归方程为 Y=6.81X+1.99×143(r=0.9995,n=6 )。线性范围 为 10~310 μg/ml,线性良好。
2.3.3 精密度试验
相对标准偏差(relative standard deviation,RSD)分别 为 0.90%,0.85%,0.88%。
2.3.4 回收率试验
配伍溶液 3 个浓度的平均回收率和 RSD 分别为 99.16% 和 0.56%,99.9% 和 0.46%,100.91% 和 0.06%。
2.3.5 Rg1 和 Re 含量比较
配伍溶液按 0,1,2,4,6 h 分别取适量样品测定,以配伍 0 h 的 Rg1 和 Re 含量为 100%,计算各时间点的相对含量,见表 2。配伍后 6 h 内参附注射液 Rg1 及 Re 含量变化均极小,并且各样本之间无显著差异。
3 讨论
本研究对参附注射液的常用临床用量中单次最大浓 度药液及单次最小浓度药液分别与复方氨基酸(18AA- Ⅶ)注射液进行配伍分析,在 23 ℃室温下观察配伍溶液外 观性状、pH、可见异物等,结果均符合药典规定。配伍后 6 h 内参附注射液两种质控物质 Rg1 及 Re 含量变化均极小, 并且各样本之间无显著差异,表明该配伍溶液可以在 6 h 内 未有化学反应和结构改变,可以配伍供临床使用。但本研 究仅考察了参附注射液与复方氨基酸(18AA- Ⅶ)注射液 配伍溶液的稳定性,尚未对参附注射液与其他药液临床可 能配伍溶液进行稳定性分析;其次,本研究仅在常温下观 察 6 h 内配伍溶液的稳定性,对其在非常温下及更长时间内 的配伍稳定性尚未作进一步考察。
[参考文献]
[1]郑曙云,徐建国,赵振中 . 参附注射液对大鼠心肌缺血再灌注损伤的影响 [J]. 中国中西医结合杂志,2004,24(6):541-544,548.
[2]徐志清,华靖,黄瑛,等 . 参附注射液治疗急性心肌梗死后急性左心衰竭疗效观察 [J]. 中国中西医结合急救杂志,2011,18(5): 287-289.
[3]贺泽龙,袁卫红,邹晓玲 . 参附注射液对充血性心力衰竭患者血流动力学的影响及机理探讨 [J]. 中国中西医结合杂志,2001, 21(5):386-387.
[4]程菲 . 复方氨基酸注射液(18AA- Ⅶ)与注射用奥美拉唑钠存在配伍禁忌 [J]. 世界最新医学信息文摘(连续型电子期刊), 2015,15(39):12.
[5]张志花,周怡 .1例复方氨基酸注射液(18AA- Ⅶ)外渗的原因分析及护理 [J]. 医学信息,2015(11):331.
[6]国家药典委员会.中华人民共和国药典(2010 年版)一部附录 [M]. 北京:化学工业出版社,2010 :28,33-34,40-41,60,61.
[7]国家药典委员会 . 中华人民共和国药典(2010 年版)一部附录 [M]. 北京:化学工业出版社,2010 :61,63,65-66,84-85.
[8]中华人民共和国卫生部药典委员会 . 中华人民共和国卫生部药品标准(中药成方制剂)第18 册参附注射液质量标准 [M]. 北京:人民卫生出版社,1998 :166-167.

欢迎关注《医疗装备》官方公众号