我要报名:报名回执表(点击下载)
医疗器械生产企业从建厂、设备验证、工艺设计、产品研发以及后续产品注册,每一阶段都是环环相扣,为得就是保证产品的生产质量,保证用械的安全。
为进一步加强我市医疗器械生产企业质量管理规范管理工作,增强企业对医疗器械相关受控环境的建设、验证以及标准理解,提高企业人员的管理能力以及相关生产和实验室工作人员的技术水平,并结合医疗器械生产质量管理规范及其附录的相关内容,我单位兹定于2019年3月12—14日在北京举办“医疗器械生产企业厂房建设阶段、设备管理阶段、产品设计研发阶段和产品注册生产阶段中需关注的问题”培训班。现就有关事宜通知如下:
一、时间地点
时间:2019年3月12—14日,会期三天。
地点:北京(具体地点将于培训前5天通过报名邮箱通知)。
二、主办单位及讲师
主办单位:医疗装备杂志社
主讲老师:
1.厂房建设阶段部分主讲老师
王坤:洁净工程领域专家。
2.厂房验证、设备管理以及产品设计相关部分主讲老师
苏建程、李婧、王霖、闵男:北京市医疗器械检验所材料三室资深检测工程师。
3.审评要点解析
王晨:北京市医疗器械审评中心资深专家。
4.飞检要点解析
刘欣:北京市药品监督管理局器械处资深专家。
三、培训内容
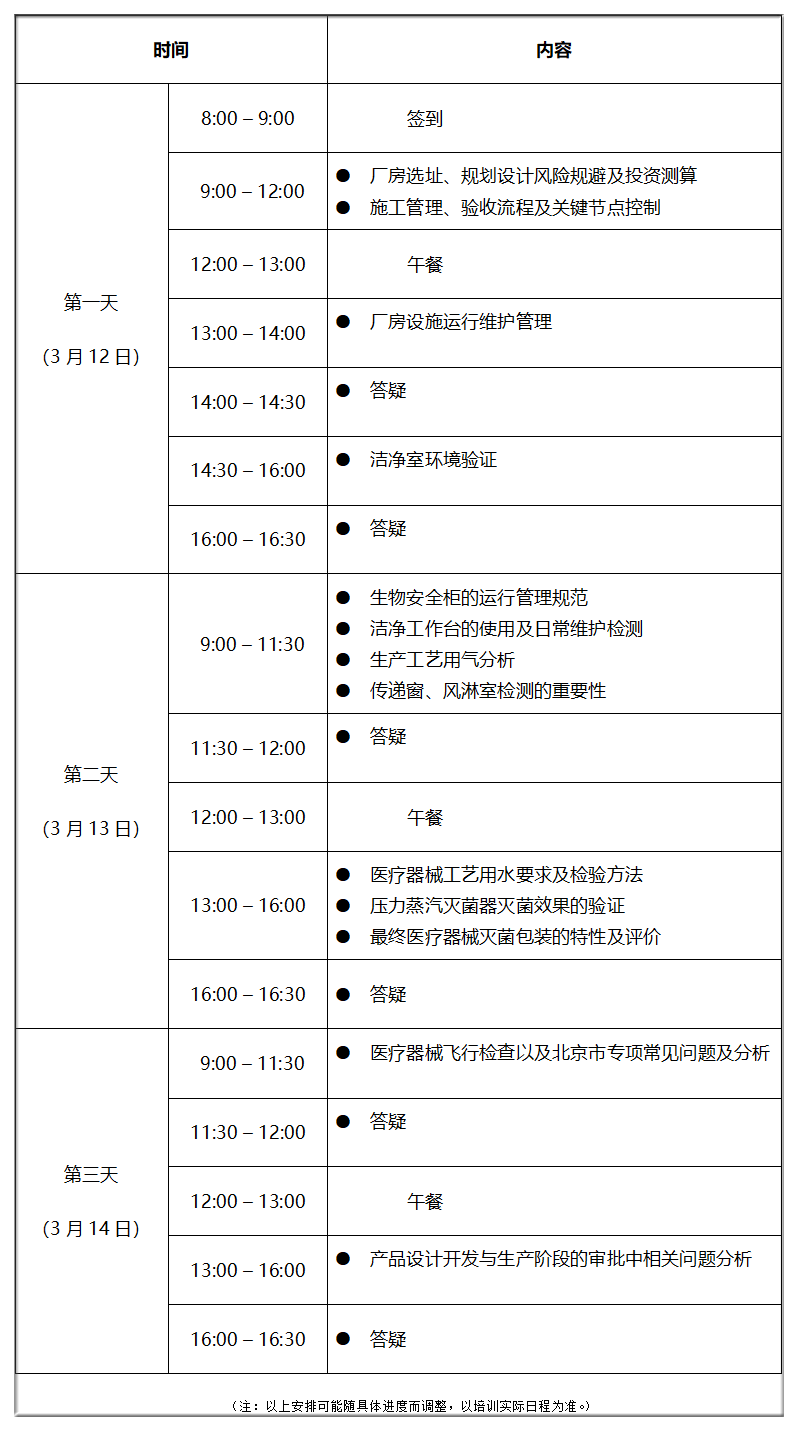
四、培训对象
无菌、植入及IVD医疗器械研发生产企业相关注册、管理和技术研发等人员。
五、培训费用
1、培训费2800元/人(包含培训资料、场地、午餐和证书等);交通、住宿等自行安排,费用自理。
2、《医疗装备》杂志理事单位首次参加可免培训费1人,超出名额享受6折优惠;已享受免费名额的理事单位报名则直接享受6折优惠。
六、联系方式
高术雨:010-62013862 18613805429
邮 箱:ylzbzzspx@163.com
请参加培训人员详细填写报名回执表(见附件),并于2019年3月1日前将回执表以邮件的形式反馈至我单位。
附件:“医疗器械生产企业厂房建设阶段、设备管理阶段、产品设计研发阶段和产品注册生产阶段中需关注的问题”培训班报名回执表

欢迎关注《医疗装备》官方公众号